Profesor Titular del Instituto de Neurociencia, de la Universidad de Valparaíso
Doctor en Ciencias, Mención Biología. U. de Chile. 1991
Información de contacto:
E-mail: david.naranjo@uv.cl
Pasaje Harrington 287, Playa Ancha. Valparaíso
Fono: (56)-(32)-2508040
Mis principales intereses históricos se centran en los canales de potasio dependientes de voltaje. Estos son proteínas de membrana presentes en casi todas las células vivas. Ellas contienen un poro selectivo de potasio que conecta ambos lados de la membrana celular. Son el objetivo de varias neurotoxinas debido a su importante papel en la excitabilidad neuronal y muscular.
 Mi investigación actual se centra en cómo los iones potasio se transportan a través del canal, cómo el canal responde a la diferencia de potencial eléctrico a través de la membrana, y cómo la caribdotoxina (CTX), una neurotoxina de escorpión, bloquea y desbloquea el canal, lo que constituye un potente modelo para estudiar las interacciones proteína-proteína. En este último caso, hemos descubierto que CTX se bambolea antes de pegarse y de despegarse.
Mi investigación actual se centra en cómo los iones potasio se transportan a través del canal, cómo el canal responde a la diferencia de potencial eléctrico a través de la membrana, y cómo la caribdotoxina (CTX), una neurotoxina de escorpión, bloquea y desbloquea el canal, lo que constituye un potente modelo para estudiar las interacciones proteína-proteína. En este último caso, hemos descubierto que CTX se bambolea antes de pegarse y de despegarse.
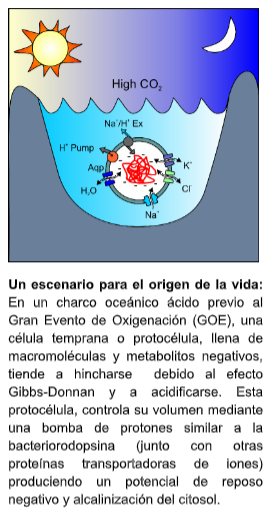
También estamos interesados en la fisiología de la membrana en las células vivas en escenarios posibles de la tierra primitiva o extraplanetarios para investigar la justificación funcional para la existencia ancestral de canales iónicos tan similares y complejos como los de nuestro cerebro. En particular, estudio el papel de los canales iónicos en el control de la hinchazón celular inducida por el efecto Gibbs-Donnan. Esta hichazón representa una amenaza constante para todas las células vivas.
Publicaciones seleccionadas:
- D. Naranjo. 2022. A scenario for the origin of life: Volume regulation by bacteriorhodopsin required extremely voltage sensitive Na-channels and very selective K-channels. BioEssays 44 (10), 2100210.
- Moldenhauer H, Díaz-Franulic I, Poblete H & D. Naranjo. 2019. Trans-toxin ion-sensitivity of charybdotoxin-blocked potassium-channels reveals unbinding transitional states. 2019. Elife. 8:e46170.
- Díaz-Franulic I, González-Pérez V, Moldenhauer H, Navarro-Quezada N & Naranjo D. 2018. Gating-induced large aqueous volumetric remodeling and aspartate tolerance in the voltage sensor domain of Shaker K+ channels. Proc Natl Acad Sci USA 115:8203-8208.
- Naranjo D , Moldenhauer H, Picuntureo M & Díaz-Franulic I.2016. Pore size matters for potassium channel conductance. The Journal of General Physiology 148:277-291.
- Díaz-Franulic I, Sepúlveda R, Navarro-Quezada N, González-Nilo F & Naranjo D. 2015. Pore dimensions and the role of occupancy in unitary conductance of Shaker K-channels. The Journal of General Physiology. 146:133-146.
- González-Pérez V, Stack K, Boric K & Naranjo D. 2010. Reduced voltage sensitivity in a K+-channel voltage sensor by electric field remodeling. Proc Natl Acad Sci USA. 107:5178-5183
- García E, Scanlon M & Naranjo D. 1999. A marine snail toxin shares with scorpion toxins a convergent mechanism of blockade on the pore of voltage-gated K channels. The Journal of General Physiology. 114:141-157.
- Naranjo D & Miller C. 1996. A strongly interacting pair of residues on the contact surface of charybdotoxin and a Shaker K+ channel. Neuron. 16:123-130
- Naranjo D, Plant C, Dunlap K & Brehm P. 1994. Two subcellular mechanisms underlie calcium-dependent facilitation of bioluminescence. Neuron. 3:1293-1301.
- Naranjo D & Brehm P. 1993. Modal shifts in acetylcholine receptor channel gating confer subunit-dependent desensitization. Science. 260:1811-1814


